Идеал хийн шинж чанарыг судлах нь физикийн чухал сэдэв юм. Хийн системийн шинж чанаруудын талаархи танилцуулга нь Бойл-Мариоттын тэгшитгэлийг авч үзэхээс эхэлдэг, учир нь энэ нь идеал хийн анхны туршилтаар нээсэн хууль юм. Үүнийг нийтлэлд илүү дэлгэрэнгүй авч үзье.
Идеал хий гэж юу гэсэн үг вэ?
Бойл-Мариотын хууль болон түүнийг тодорхойлсон тэгшитгэлийн талаар ярихаасаа өмнө идеал хийг тодорхойлъё. Үүнийг бүрдүүлэгч хэсгүүд нь хоорондоо харилцан үйлчлэлцдэггүй, хэмжээ нь бөөмс хоорондын дундаж зайтай харьцуулахад өчүүхэн бага байдаг шингэн бодис гэж ерөнхийд нь ойлгодог.
Үнэндээ аливаа хий бодит, өөрөөр хэлбэл түүнийг бүрдүүлэгч атом, молекулууд нь тодорхой хэмжээтэй, ван дер Ваалсын хүчний тусламжтайгаар бие биетэйгээ харилцан үйлчилдэггүй. Гэсэн хэдий ч өндөр үнэмлэхүй температур (300 К-ээс дээш) ба нам даралт (нэг атмосферээс бага) үед атом ба молекулуудын кинетик энерги нь ван дер Ваалсын харилцан үйлчлэлийн энергиээс хамаагүй өндөр байдаг тул бодит хий заасан үед.өндөр нарийвчлалтай нөхцөлийг хамгийн тохиромжтой гэж үзэж болно.
Бойл-Мариотын тэгшитгэл
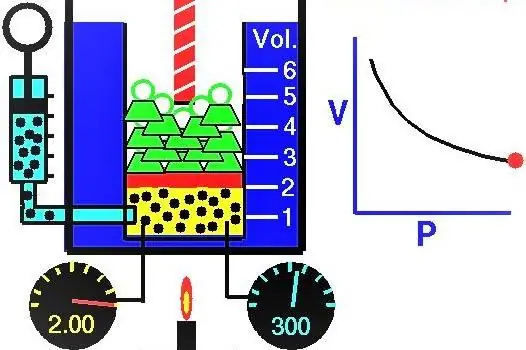
Хийн шинж чанарууд Европын эрдэмтэд XVII-XIX зууны үед идэвхтэй судалж байжээ. Туршилтаар нээсэн хамгийн анхны хийн хууль бол хийн системийн тэлэлт, шахалтын изотерм процессыг тодорхойлсон хууль юм. Холбогдох туршилтуудыг 1662 онд Роберт Бойл, 1676 онд Эдм Мариотт нар хийсэн. Эдгээр эрдэмтэд тус бүр хаалттай хийн систем дэх изотермийн процессын үед даралт нь эзэлхүүнээсээ урвуу байдлаар өөрчлөгддөг болохыг бие даан харуулсан. Туршилтаар олж авсан процессын математик илэрхийллийг дараах хэлбэрээр бичнэ:
PV=k
П ба V нь систем дэх даралт ба түүний эзэлхүүн бол k нь хийн бодисын хэмжээ ба түүний температураас хамаардаг зарим тогтмол юм. Хэрэв та график дээр P(V) функцийн хамаарлыг бий болговол энэ нь гипербол болно. Эдгээр муруйнуудын жишээг доор харуулав.
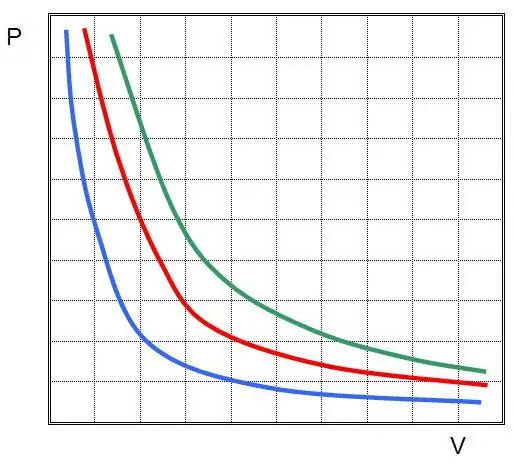
Бичсэн тэгш байдлыг Бойл-Мариотын тэгшитгэл (хууль) гэж нэрлэдэг. Энэ хуулийг товчоор дараах байдлаар томъёолж болно: тогтмол температурт хамгийн тохиромжтой хийн тэлэлт нь түүний доторх даралтыг пропорциональ бууруулахад хүргэдэг, харин эсрэгээр хийн системийн изотермийн шахалт нь түүний доторх даралтын пропорциональ өсөлт дагалддаг.
Хамгийн тохиромжтой хийн тэгшитгэл
Бойл-Мариоттын хууль нь Менделеев ба нэрийг агуулсан илүү ерөнхий хуулийн онцгой тохиолдол юм. Клапейрон. Эмиль Клапейрон 1834 онд янз бүрийн гадаад нөхцөлд хийн төлөв байдлын талаархи туршилтын мэдээллийг нэгтгэн дүгнэж, дараах тэгшитгэлийг олж авсан:
PV=nRT
Өөрөөр хэлбэл хийн системийн V эзэлхүүний үржвэр ба түүний доторх P даралтын үржвэр нь абсолют температур T ба n бодисын хэмжээний үржвэртэй шууд пропорциональ байна. Энэ пропорциональ байдлын коэффициентийг R үсгээр тэмдэглэж, хийн бүх нийтийн тогтмол гэж нэрлэдэг. Бичсэн тэгшитгэлд R-ийн утга нь 1874 онд Дмитрий Иванович Менделеевийн хийсэн олон тооны тогтмолыг сольсны улмаас гарч ирсэн.
Төлөвийн бүх нийтийн тэгшитгэлээс харахад температурын тогтмол байдал ба бодисын хэмжээ нь тэгшитгэлийн баруун талын өөрчлөгдөөгүй байдлыг баталгаажуулдаг бөгөөд энэ нь тэгшитгэлийн зүүн тал мөн тогтмол хэвээр байх болно гэсэн үг юм.. Энэ тохиолдолд бид Бойл-Мариотын тэгшитгэлийг авна.

Хийн бусад хууль
Дээрх догол мөрөнд бичсэн Клапейрон-Менделеевийн тэгшитгэл нь P, V, T гэсэн гурван термодинамик параметрийг агуулна. Хэрэв тэдгээр нь тус бүр тогтмол, нөгөө хоёр нь өөрчлөгдөхийг зөвшөөрвөл Бойл-Мариотт, Чарльз ба Гэй-Люссакийн тэгшитгэл. Чарльзын хууль нь изобар процессын эзэлхүүн ба температурын шууд пропорциональ байдлын тухай өгүүлдэг ба Гэй-Люссакийн хуульд изохорик шилжилтийн үед хийн даралт нь үнэмлэхүй температуртай шууд пропорциональ өсөж, буурдаг гэж заасан байдаг. Харгалзах тэгшитгэлүүд дараах байдалтай байна:
V/T=const үед P=const;
P/T=const үед V=const.
ТэгэхээрТиймээс Бойл-Мариоттын хууль нь хийн гурван үндсэн хуулийн нэг юм. Гэхдээ график хамаарлаараа бусдаас ялгаатай: V(T) ба P(T) функцууд нь шулуун шугам, P(V) функц нь гипербол.
Бойл-Мариотын хуулийг хэрэгжүүлэх даалгаврын жишээ
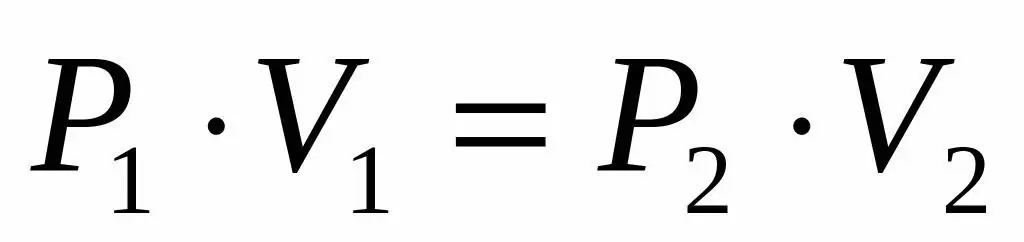
Анхны байрлал дахь поршений доорх цилиндр дэх хийн эзэлхүүн 2 литр, даралт нь 1 атмосфер байв. Поршен нэмэгдэж, хийн системийн эзэлхүүн 0.5 литрээр нэмэгдсэний дараа хийн даралт ямар байсан бэ. Уг процессыг изотерм гэж үзнэ.
Идеал хийн даралт ба эзэлхүүнийг бидэнд өгсөн ба түүнийг тэлэх явцад температур өөрчлөгдөөгүй гэдгийг бид мэддэг тул Бойл-Мариотын тэгшитгэлийг дараах хэлбэрээр ашиглаж болно:
P1V1=P2V 2
Энэ тэгшитгэл нь өгөгдсөн температур дахь хийн төлөв бүрийн хувьд эзэлхүүн-даралтын бүтээгдэхүүн тогтмол байна. Тэгш байдлын P2 утгыг илэрхийлснээр бид эцсийн томъёог олж авна:
P2=P1V1/V 2
Даралтын тооцоо хийхдээ энэ тохиолдолд системээс гадуурх нэгжүүдийг ашиглаж болно, учир нь литр нь багасч, бид агаар мандалд P2даралтыг авна. Нөхцөл байдлын өгөгдлийг орлуулснаар бид асуудлын асуултын хариултанд хүрнэ: P2=0.8 атмосфер.






