Альдегид нь -CH функциональ бүлэг агуулсан карбонилийн нэгдлүүдтэй холбоотой органик бодис бөгөөд үүнийг карбонилийн бүлэг гэж нэрлэдэг.
Молекулын нүүрсустөрөгчийн араг ясны шинж чанараас хамааран альдегид нь ханасан, ханаагүй, үнэрт байдаг. Тэдний молекулууд нь галоген атомууд эсвэл нэмэлт функциональ бүлгүүдийг агуулж болно. Ханасан альдегидийн ерөнхий томьёо нь C H2 O. IUPAC нэр томъёоны дагуу тэдний нэр нь -al.
дагавараар төгсдөг.
Альдегидийн исэлдэлт нь карбоксилын хүчилд амархан хувирдаг тул үйлдвэрлэлд чухал ач холбогдолтой. Энэ тохиолдолд зэсийн гидроксид, мөнгөний исэл эсвэл бүр агаар мандлын хүчилтөрөгч нь исэлдүүлэгч бодис болж чадна.
Карбонил бүлгийн бүтэц
С=О бүлгийн давхар бондын электрон бүтэц нь нэг σ-бонд, нэг π-бонд үүсэхээр тодорхойлогддог. С атом нь sp2-эрлийзжсэн төлөвт байгаа ба хавтгай молекул бөгөөд ойролцоогоор 1200 бондын хоорондох холбоосын өнцөгтэй. Энэ функциональ бүлгийн давхар бондын ялгаа нь нүүрстөрөгчийн атом ба өндөр электрон сөрөг хүчилтөрөгчийн атомын хооронд байрладагт оршино. Үр дүнд ньэлектронууд O атом руу татагддаг бөгөөд энэ нь энэ холбоо маш хүчтэй туйлширсан гэсэн үг.
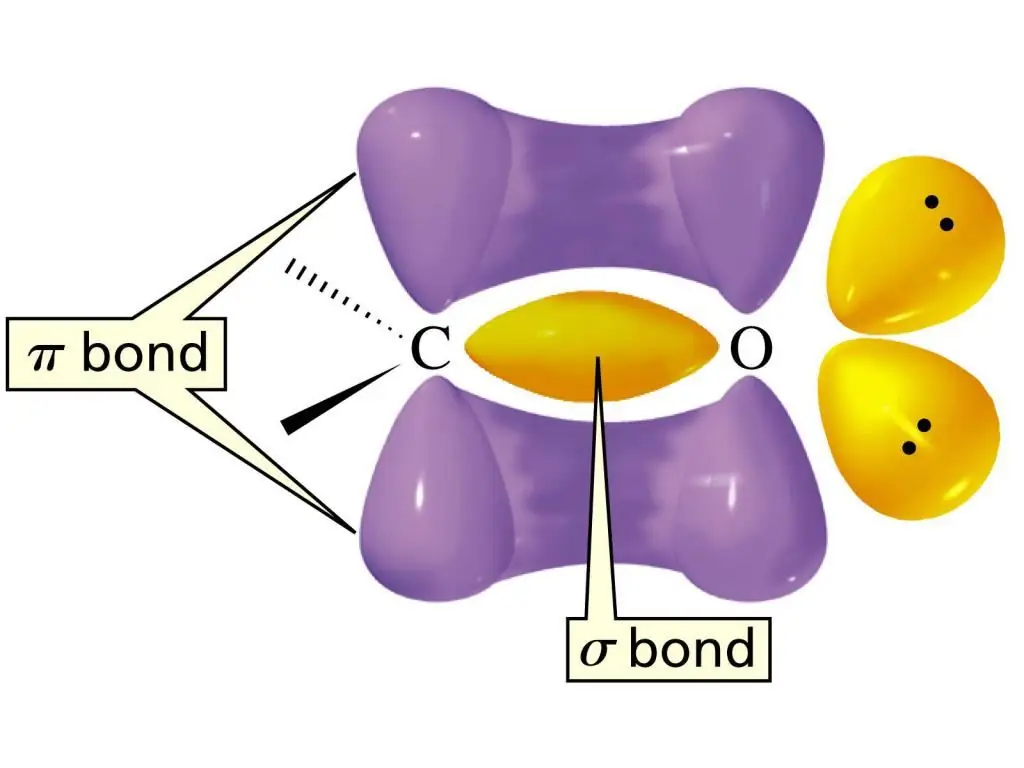
Альдегидийн бүлэгт ийм туйлширсан давхар бондын агуулгыг альдегидийн өндөр урвалын гол шалтгаан гэж нэрлэж болно. Альдегидийн хувьд атомууд эсвэл тэдгээрийн бүлгүүдийг C=O холбоонд нэмэх урвалууд хамгийн онцлог шинж чанартай байдаг. Мөн нуклеофилийн нэмэлт урвал нь үргэлжлэхэд хамгийн хялбар байдаг. Альдегидийн хувьд функциональ бүлгийн H атомуудын оролцоотой урвалууд нь альдегидийн хувьд түгээмэл байдаг. C=O бүлгийн электрон татах нөлөөгөөр бондын туйлшрал нэмэгддэг. Энэ нь эргээд альдегидийн харьцангуй хялбар исэлдэлтийн шалтгаан болдог.
Альдегидийн зарим төлөөлөгчид
Формальдегид (формальдегид эсвэл метанал) CH2O нь маш хурц үнэртэй хийн бодис бөгөөд ихэвчлэн метанолын уурыг агаартай хольж улаанаар дамжуулж гаргаж авдаг. -зэс эсвэл мөнгөн торны халуун тор. Түүний 40% усан уусмалыг формалин гэж нэрлэдэг. Формальдегид нь урвалд амархан ордог бөгөөд тэдгээрийн ихэнх нь хэд хэдэн чухал бодисын үйлдвэрлэлийн синтезийн үндэс болдог. Түүнчлэн изопрен резин, пентаэритритол, олон төрлийн эмийн бодис, төрөл бүрийн будагч бодис, арьс идээлэх, ариутгагч, үнэр дарагч бодис болгон ашигладаг. Формальдегид нь нэлээд хортой, агаар дахь MPC нь 0.001 мг/л.
Ацетальдегид (цууны альдегид, этанал) CH3SON нь амьсгал боогдуулах үнэртэй өнгөгүй шингэн бөгөөд усаар шингэлэхэд үүсдэг.жимсний үнэр. Ацетальдегид нь альдегидийн бүх үндсэн шинж чанартай байдаг. Ацетальдегидийн исэлдэлт нь асар их хэмжээний цууны хүчил ба цууны ангидрид, олон төрлийн эмийн бодисыг үүсгэдэг.
Acrolein (propenal) CH2=CH-SON, хамгийн энгийн ханаагүй альдегид нь өнгөгүй, дэгдэмхий шингэн юм. Түүний уур нь нүд, амьсгалын дээд замын салст бүрхэвчийг хүчтэй цочроодог. Маш хортой, агаарт агуулагдах MPC нь 0.7 мг/м3 байна. Пропенал нь тодорхой полимерүүдийн нийлэгжилтэнд ордог завсрын бүтээгдэхүүн бөгөөд зарим эм үйлдвэрлэхэд шаардлагатай байдаг.

Бензалдегид (бензойн альдегид) С6Н5SON нь гашуун бүйлсний амттай, хадгалах явцад шар өнгөтэй болдог өнгөгүй шингэн юм. Энэ нь агаарт маш хурдан исэлдэж, бензойн хүчилд ордог. Ургамлын эфирийн тос (нероли, пачули), глюкозид хэлбэрээр - гашуун бүйлс, интоор, чангаанз, тоор зэрэг ургамлын үрийн цөмд агуулагддаг. Анхилуун үнэртэй бодис болохын хувьд үнэртэй ус үйлдвэрлэх, хүнсний эссэнсийн бүрдэл хэсэг, бусад анхилуун үнэрт бодис (cinnamaldehyde, jasminaldehyde) нийлэгжүүлэх түүхий эд болгон ашигладаг.
Мөнгөн толины урвал
Альдегидийг мөнгөний ислээр исэлдүүлэх нь функциональ бүлгийн харгалзах хэлбэрт үзүүлэх хамгийн чухал чанарын урвал юм. Энэ урвалын явцад үүссэн туршилтын хоолойн ханан дээрх нимгэн мөнгөн бүрхүүлийн улмаас энэ урвал нэрээ авсан.
Түүний мөн чанар нь R-COH альдегидийн аммиакийн оксидын уусмалтай харилцан үйлчлэлцэхэд оршдог.мөнгө(I) нь уусдаг нийлмэл нэгдэл [Ag(NH3)2]OH ба Толленсийн урвалж гэж нэрлэгддэг. Урвалыг ус буцалгах цэгтэй ойролцоо температурт (80-100 ° C) гүйцэтгэдэг. Энэ тохиолдолд альдегидийг харгалзах карбоксилын хүчил болгон исэлдүүлж, исэлдүүлэгч бодисыг металл мөнгө болгон бууруулж тунадас үүсгэдэг.
Урвалж бэлтгэх
Альдегид дэх -SON бүлгийг чанарын хувьд тодорхойлохын тулд эхлээд мөнгөний нэгдэл бэлтгэдэг. Үүнийг хийхийн тулд аммиакийн (аммиакийн гидроксид) бага зэрэг уусмалыг туршилтын хоолойд хийнэ, дараа нь бага хэмжээний мөнгөний нитрат хийнэ. Энэ тохиолдолд үүссэн мөнгөний ислийн тунадас шууд алга болно:
2AgNO3 + 2NH3 + H2O -> Ag 2O↓ + 2NH4NO3
Ag2O + 4NΗ3 + Η2O -> 2[Ag (NΗ3)2]ОΗ
Шүлтээр бэлтгэсэн Толленсын урвалж илүү найдвартай үр дүнг өгдөг. Үүнийг хийхийн тулд 1 г AgNO3 10 г нэрмэл усанд уусгаж, ижил хэмжээний концентрацитай натрийн гидроксид нэмнэ. Үүний үр дүнд Ag2O-ийн тунадас үүсч, аммонийн гидроксидын концентрацитай уусмал нэмэхэд алга болно. Урвалын хувьд зөвхөн шинэхэн бэлтгэсэн урвалжийг ашиглах ёстой.

Урвалын механизм
Мөнгөн толины урвал нь тэгшитгэлтэй тохирч байна:
2[Ag(NΗ3)2]OΗ + НСОΗ-> 2Ag↓ + ΗCOONΗ4 + 3NΗ3 + H2O
Альдегидийн хувьд энэ харилцан үйлчлэл хангалттай судлагдаагүй байгааг тэмдэглэх нь зүйтэй. Энэ урвалын механизм тодорхойгүй боловч радикал эсвэл ионы исэлдэлтийн хувилбар гэж үздэг. Диаммин мөнгөний гидроксид нь диолын мөнгөний давсыг үүсгэснээр нэмэгддэг бөгөөд үүнээс мөнгө задарч карбоксилын хүчил үүсгэдэг.
Ашиглаж буй багаж хэрэгслийн цэвэр байдал нь туршилтыг амжилттай явуулахад маш чухал. Энэ нь туршилтын явцад үүссэн коллоид мөнгөний тоосонцор нь шилний гадаргууд наалдаж, толин тусгал гадаргуу үүсгэдэгтэй холбоотой юм. Бага зэргийн бохирдол байгаа тохиолдолд саарал өнгийн тунадас хэлбэрээр тунадас орно.
Савыг цэвэрлэхийн тулд шүлтийн уусмал хэрэглэнэ. Тиймээс, эдгээр зорилгоор та NaOH-ийн уусмалыг авч болно, үүнийг их хэмжээний нэрмэл усаар зайлж угаана. Шилэн гадаргуу нь өөх тос, механик тоосонцоргүй байх ёстой.
Зэсийн гидроксидээр исэлдүүлэх
Альдегидийг зэс (II) гидроксидтэй исэлдүүлэх урвал нь функциональ бүлгийн төрлийг тодорхойлоход нэлээд үр дүнтэй бөгөөд үр дүнтэй байдаг. Энэ нь урвалын хольцыг буцалгахад тохирох температурт явагддаг. Үүний зэрэгцээ альдегид нь Фелингийн урвалж дахь хоёр валенттай зэсийг (Cu(OH)2 шинэхэн бэлтгэсэн аммиакийн уусмал) нэг валенттай зэс болгон бууруулдаг. C-H холбоонд хүчилтөрөгчийн атом орсны улмаас тэд өөрсдөө исэлддэг (С-ийн исэлдэлтийн төлөв +1-ээс +3 хүртэл өөрчлөгддөг).
Хөдөлгөөний ард харагдах байдалуусмалын хольцын өнгийг өөрчлөх замаар урвалыг ажиглаж болно. Зэсийн гидроксидын хөхөвтөр тунадас аажмаар шар болж, нэг валент зэсийн гидроксид таарч, Cu2O.
тод улаан тунадас үүснэ.
Энэ процесс нь урвалын тэгшитгэлтэй тохирч байна:
R-SLEEP + Cu2+ + NaOH + H2O -> R-COONa + Cu 2O + 4H+

Жонсын урвалжтай үйлдэл
Ийм урвалж нь альдегид дээр хамгийн сайнаар нөлөөлдөг гэдгийг тэмдэглэх нь зүйтэй. Энэ тохиолдолд исэлдэлт нь халаалт шаарддаггүй бөгөөд 0-20 ° C-ийн температурт нэлээд богино хугацаанд хийгддэг бөгөөд бүтээгдэхүүний гарц нь 80% -иас дээш байдаг. Жонс урвалжийн гол сул тал нь бусад функциональ бүлгүүдийн хувьд өндөр сонгомол чанар байхгүйгээс гадна хүчиллэг орчин нь заримдаа изомержих эсвэл устгахад хүргэдэг.
Жонс урвалж нь хромын (VI) ислийн шингэрүүлсэн хүхрийн хүчил ба ацетон дахь уусмал юм. Үүнийг натрийн бихроматаас ч авч болно. Альдегидийг исэлдүүлэх үед энэ урвалжийн нөлөөгөөр карбоксилын хүчил үүсдэг.
Үйлдвэрийн хүчилтөрөгчийн исэлдэлт
Аж үйлдвэрт ацетальдегидийг исэлдүүлэх нь катализатор болох кобальт эсвэл манганы ионуудын дэргэд хүчилтөрөгчийн үйлчлэлээр явагддаг. Перацетик хүчил эхлээд үүсдэг:
CH3-УНТАХ + O2 -> CH3-UNOH
Тэр нь эргээд ацетальдегидийн хоёр дахь молекул болон хэт ислээр харилцан үйлчилдэг.нэгдэл нь цууны хүчлийн хоёр молекулыг өгдөг:
CH3-COOH + CH3-SON -> 2CH3-COOH
Исэлдэлтийг 60-70 °C температурт, 2 105 Па.
даралттай хийнэ.
Иодын уусмалтай харилцан үйлчлэл
Альдегидийн бүлгүүдийг исэлдүүлэхийн тулд заримдаа шүлттэй иодын уусмалыг хэрэглэдэг. Энэхүү урвалж нь нүүрс усны исэлдэлтийн процесст онцгой ач холбогдолтой бөгөөд учир нь энэ нь маш сонгомол байдлаар ажилладаг. Тиймээс түүний нөлөөн дор D-глюкоз нь D-глюконы хүчил болж хувирдаг.
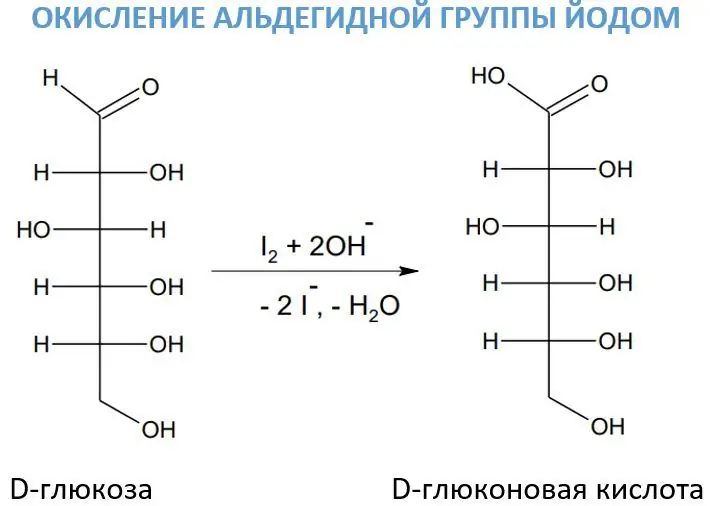
Иод нь шүлтлэг байлцуулан гипоиодид (маш хүчтэй исэлдүүлэгч бодис) үүсгэдэг:.
Гипиоодидын үйлчлэлээр формальдегид нь метан хүчил болж хувирдаг: ΗСОΗ + NaIO + NaOΗ -> ΗCOONa + NaI + H2O.
Альдегидийн иодын исэлдэлтийг аналитик химид тэдгээрийн уусмал дахь тоон хэмжээг тодорхойлоход ашигладаг.
Селений давхар ислээр исэлдүүлэх
Өмнөх урвалжуудаас ялгаатай нь селенийн давхар ислийн нөлөөгөөр альдегид нь дикарбонилийн нэгдэл болж хувирч, формальдегидээс глиоксал үүсдэг. Хэрэв метилен эсвэл метилийн бүлгүүд карбонилийн хажууд байрладаг бол тэдгээр нь карбонил болж хувирдаг. SeO2-ийн уусгагч болгон ихэвчлэн диоксан, этанол эсвэл ксилолыг ашигладаг.
Нэг аргын дагуу урвалыг хутгагч, термометр, рефлюкс конденсатортой холбосон гурван хүзүүтэй колбонд хийнэ. 0.25 моль-ийн хэмжээгээр авсан эхлэлийн материалд дуслаар уусмал нэмнэ180 мл диоксанд 0.25 моль селенийн давхар исэл, түүнчлэн 12 мл H2O. Температур нь 20 ° C-аас хэтрэхгүй байх ёстой (шаардлагатай бол колбыг хөргөнө). Үүний дараа байнгын хутгах замаар уусмалыг 6 цагийн турш буцалгана. Дараа нь халуун уусмалыг шүүж, селен ялгаж, тунадасыг диоксанаар угаана. Уусгагчийг вакуум нэрэлтийн дараа үлдэгдэл нь хуваагдана. Үндсэн фракцыг өргөн температурт (20-30 °C) авч, дахин засна.
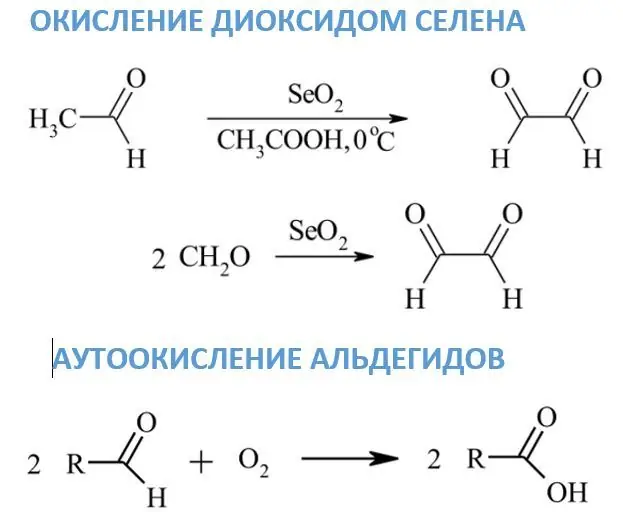
Альдегидийн автомат исэлдэлт
Тасалгааны температурт агаар мандлын хүчилтөрөгчийн нөлөөн дор альдегидийн исэлдэлт маш удаан явагддаг. Эдгээр урвалын гол бүтээгдэхүүн нь харгалзах карбоксилын хүчил юм. Авто исэлдэлтийн механизм нь этаналыг цууны хүчилд үйлдвэрлэлийн исэлдүүлэхтэй холбоотой юм. Завсрын бүтээгдэхүүний нэг нь өөр альдегидийн молекултай урвалд ордог перацид юм.
Энэ төрлийн урвалыг гэрэл, хэт исэл, хүнд металлын ул мөр түргэсгэдэг тул түүний радикал механизмтай гэж дүгнэж болно. Усан уусмалд агуулагдах формальдегид нь устай метилен гликол хэлбэрээр агуулагддаг тул агаарт аналогиасаа хамаагүй муу исэлддэг.

Альдегидийг калийн перманганатаар исэлдүүлэх
Энэ урвал нь хүчиллэг орчинд хамгийн амжилттай явагддаг. Калийн перманганатын уусмалын эрчмийг алдах, ягаан өнгө бүрэн алдагдах зэргээр түүний дамжуулалтыг нүдээр үнэлэх боломжтой. Урвал нь цагт явагданаөрөөний температур, хэвийн даралттай тул тусгай нөхцөл шаарддаггүй. Туршилтын хоолойд 2 мл формальдегид, хүхрийн хүчлээр хүчиллэгжүүлсэн калийн перманганатын 1 мл уусмал асгахад хангалттай. Туршилтын хоолойг уусмалаар зөөлөн сэгсэрч урвалжуудыг холино:
5CH3-УНТАХ + 2KMnO4 + 3Ц2SO 4 =5CH3-COOH + 2MnSO4 + K2SO 4 + 3H2O
Хэрэв ижил урвалыг өндөр температурт хийвэл метанал нүүрстөрөгчийн давхар исэл болж амархан исэлддэг:
5CH3-УНТАХ + 4KMnO4 + 6H2SO 4 =5SO2 + 4MnSO4 + 2K2SO 4 + 11Н2O






