Молекул-кинетик онол нь системийн микроскопийн үйл ажиллагаанд дүн шинжилгээ хийж, статистик механикийн аргуудыг ашиглан термодинамик системийн макроскопийн чухал шинж чанарыг олж авах боломжийг олгодог. Системийн температуртай холбоотой микроскоп шинж чанаруудын нэг нь хийн молекулуудын дундаж квадрат хурд юм. Бид түүний томъёог өгч, нийтлэлд авч үзэх болно.
Хамгийн тохиромжтой бензин
Хийн молекулуудын квадрат дундаж хурдны томъёог тусгайлан идеал хийн хувьд өгөх болно гэдгийг бид шууд тэмдэглэж байна. Үүний дагуу физикийн хувьд бөөмс (атом, молекул) нь хоорондоо харилцан үйлчлэлцдэггүй (тэдгээрийн кинетик энерги нь харилцан үйлчлэлийн боломжит энергиэс хэд хэдэн хэмжигдэхүүнээр давж гардаг), хэмжээсгүй, ийм олон бөөмсийн системийг авч үздэг. өөрөөр хэлбэл тэдгээр нь хязгаарлагдмал масстай цэгүүд (хэмжээнээс хэд хэдэн дарааллаар их хэмжээний бөөмс хоорондын зай).шугаман).
Химийн хувьд төвийг сахисан молекулууд эсвэл атомуудаас бүрдэх, бага даралттай, өндөр температуртай аливаа хийг хамгийн тохиромжтой гэж үзэж болно. Жишээлбэл, агаар бол хамгийн тохиромжтой хий боловч усны уур нь тийм биш болсон (устөрөгчийн молекулуудын хооронд хүчтэй устөрөгчийн холбоо үйлчилдэг).
Молекул кинетик онол (MKT)

МКТ-ийн хүрээнд хамгийн тохиромжтой хийг судлахдаа хоёр чухал процессыг анхаарах хэрэгтэй:
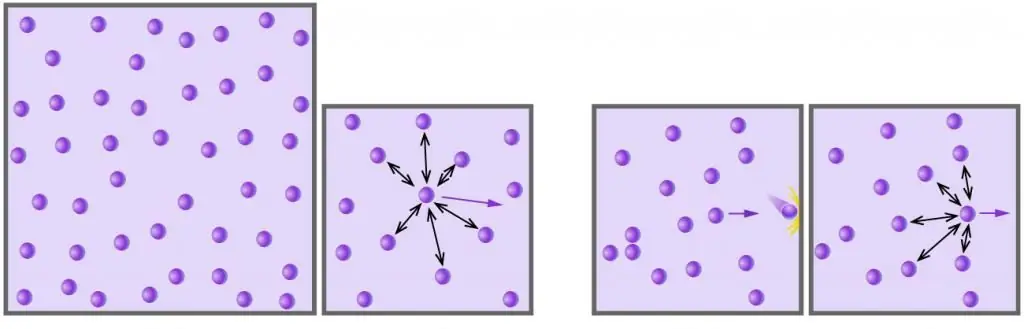
- Хий нь молекул, атомууд мөргөлдөх импульсийг агуулсан савны хананд шилжиж даралт үүсгэдэг. Ийм мөргөлдөөн нь төгс уян хатан байдаг.
- Хийн молекулууд болон атомууд янз бүрийн хурдтайгаар бүх чиглэлд санамсаргүй байдлаар хөдөлдөг бөгөөд тархалт нь Максвелл-Больцманы статистикт захирагддаг. Бөөмүүдийн хооронд мөргөлдөх магадлал маш бага, учир нь тэдгээр нь өчүүхэн хэмжээтэй, тэдгээрийн хоорондох зай ихтэй байдаг.
Хийн хэсгүүдийн бие даасан хурд нь бие биенээсээ эрс ялгаатай хэдий ч системд гадны нөлөөлөл байхгүй тохиолдолд энэ утгын дундаж утга цаг хугацааны явцад тогтмол хэвээр байна. Хийн молекулуудын дундаж квадрат хурдны томьёог кинетик энерги ба температурын хамаарлыг авч үзэж болно. Бид нийтлэлийн дараагийн догол мөрөнд энэ асуудлыг авч үзэх болно.
Идеал хийн молекулуудын квадрат дундаж хурдны томъёоны гарал үүсэл
Оюутан бүр физикийн ерөнхий хичээлээс m масстай биеийн хөрвүүлэх хөдөлгөөний кинетик энергийг дараах байдлаар тооцдогийг мэддэг:
Ek=mv2/2
Энд v нь шугаман хурд юм. Нөгөөтэйгүүр бөөмийн кинетик энергийг мөн kB хувиргах коэффициентийг (Больцманы тогтмол) ашиглан абсолют температурын T-ээр тодорхойлж болно. Манай орон зай гурван хэмжээст тул Ek-г дараах байдлаар тооцно:
Ek=3/2kBT.
Тэнцүү байдлын аль алиных нь адил тэнцүү ба тэдгээрээс v-г илэрхийлбэл квадрат идеал хийн дундаж хурдны томъёог олж авна:
mv2/2=3/2kBT=>
v=√(3kBT/m).
Энэ томъёонд m - хийн бөөмийн масс юм. Энэ нь бага (≈ 10-27кг) тул практик тооцоонд ашиглахад тохиромжгүй. Энэхүү таагүй байдлаас зайлсхийхийн тулд бүх нийтийн хийн тогтмол R ба молийн масс M-ийг эргэн санацгаая. kB-тай R тогтмол нь тэгшитгэлээр холбогдоно:
kB=R/NA.
M-ийн утгыг дараах байдлаар тодорхойлно:
M=mNA.
Хоёр тэгш байдлыг харгалзан бид молекулуудын язгуур дундаж квадрат хурдны дараах илэрхийллийг олж авна:
v=√(3RT/M).
Тиймээс хийн хэсгүүдийн дундаж квадрат хурд нь үнэмлэхүй температурын квадрат язгууртай шууд пропорциональ, молийн массын квадрат язгууртай урвуу пропорциональ байна.
Асуудлыг шийдвэрлэх жишээ
Бидний амьсгалж буй агаар 99% азот ба хүчилтөрөгч гэдгийг хүн бүр мэддэг. 15 o температурт N2 ба O2 молекулуудын дундаж хурдны ялгааг тодорхойлох шаардлагатай. C.

Энэ асуудлыг дараалан шийдвэрлэх болно. Эхлээд бид температурыг үнэмлэхүй нэгж болгон хөрвүүлбэл:
T=273, 15 + 15=288, 15 К.
Одоо авч үзэж буй молекул бүрийн молийн массыг бичнэ үү:
MN2=0.028 кг/моль;
MO2=0.032 кг/моль.
Молийн массын утга бага зэрэг ялгаатай тул ижил температурт тэдгээрийн дундаж хурд нь ойролцоо байх ёстой. v-ийн томъёог ашиглан бид азот ба хүчилтөрөгчийн молекулуудын дараах утгыг олж авна:
v (N2)=√(38, 314288, 15/0, 028)=506.6 м/с;
v (O2)=√(38, 314288, 15/0, 032)=473.9 м/с.
Азотын молекулууд хүчилтөрөгчийн молекулуудаас арай хөнгөн тул илүү хурдан хөдөлдөг. Дундаж хурдны зөрүү:
v (N2) - v (O2)=506.6 - 473.9=32.7 м/ с.
Үйлдвэрлэлийн утга нь азотын молекулуудын дундаж хурдны ердөө 6.5% л байна. Бид бага температурт ч гэсэн хий дэх молекулуудын өндөр хурдыг анхаарч үздэг.






